Neovascolarizzazione/Angiogenesi
![]()
PSI per neovascolarizzazione/angiogenesi
La neurovascolarizzazione è la formazione di nuove reti microvascolari. In vivo, questo processo si ottiene principalmente tramite angiogenesi, la gemmazione di nuovi vasi da vasi esistenti. La neovascolarizzazione/angiogenesi gioca un ruolo essenziale in diverse terapie e patologie ed è per questo che viene studiata in maniera approfondita in diversi ambiti quali medicina rigenerativa e ingegneria dei tessuti, biologia vascolare e biologia dei tumori. Esistono diversi modelli, a seconda dell’applicazione, per sviluppo/fornitura di farmaci, caratterizzazione delle patologie e trattamento delle cellule staminali. Sono necessari strumenti utilizzabili per la valutazione della formazione di nuovi vasi, preferibilmente tramite metodi non invasivi e non distruttivi. Il sistema PeriCam PSI con laser speckle contrast imaging può essere utilizzato per misurare le variazioni nella perfusione sanguigna microvascolare nel tempo. Alcuni studi hanno mostrato che gli incrementi della perfusione corrispondono a una formazione di vasi sanguigni più funzionale. PeriCam PSI è stato utilizzato in diversi modelli di questo tipo.
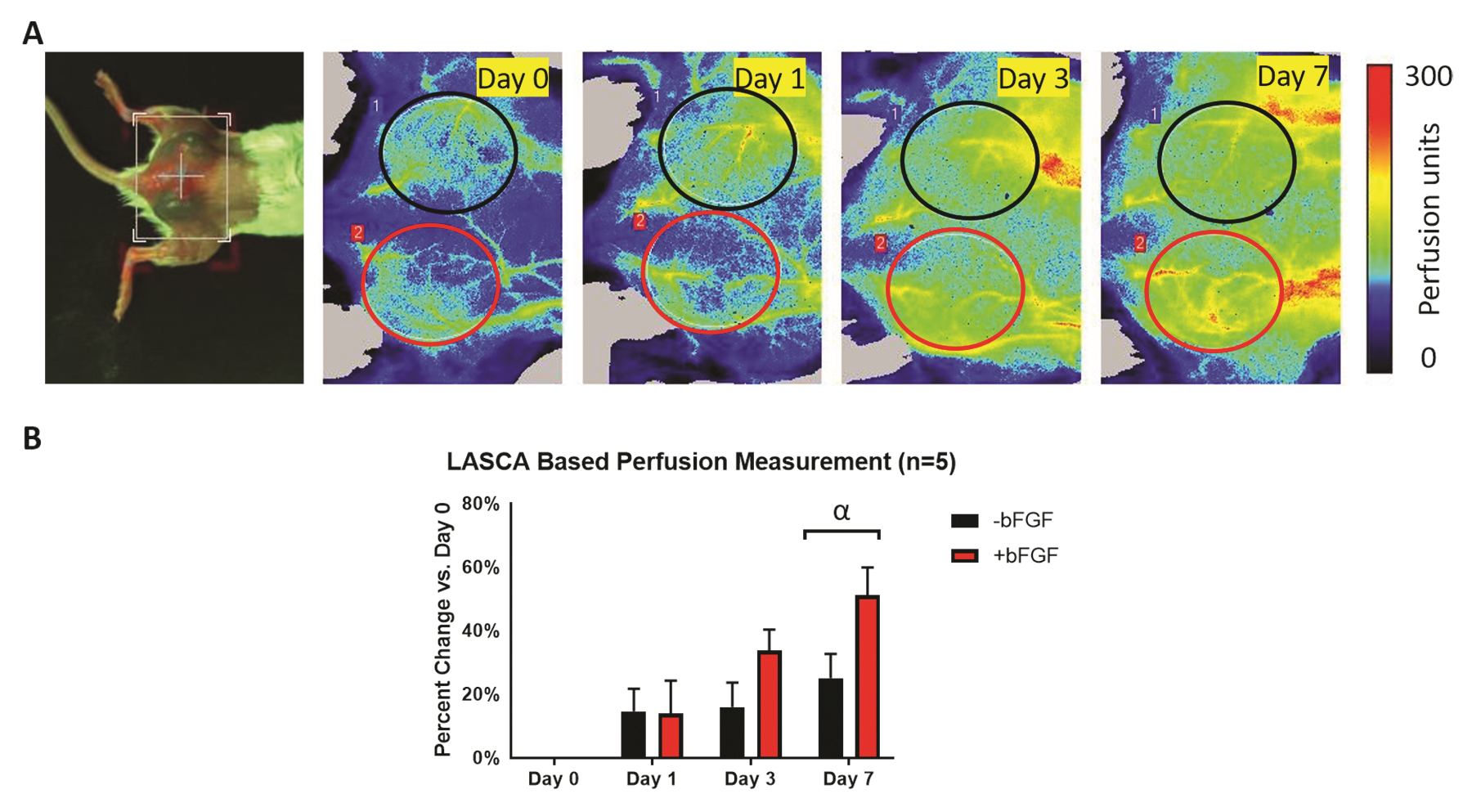
(A) Foto della vista dorsale e delle immagini di perfusione PSI longitudinali di un topo con due impianti di scaffold con fibrina sottocutanea con e senza fattore di crescita angiogenici. Le ROI sono state scelte in base alla posizione fisica degli impianti. (B) La quantificazione della variazione della perfusione relativa al giorno 0, in base all’analisi della ROI delle immagini di perfusione PSI, mostra l’incremento complessivo della perfusione nel tempo. La variabilità massima della perfusione è stata osservata il giorno 7, con scaffold +bFGF che tendevano a una perfusione maggiore rispetto a scaffold -bFGF 1-2.
Immagine per gentile concessione del dott. Mario Fabiilli da LED-Based Photoacoustic Imaging for Monitoring Angiogenesis in Fibrin Scaffolds Autore: Yunhao Zhu, Xiaofang Lu, Xiaoxiao Dong, et al Publication: Tissue Engineering Part C: Methods
Publisher: Mary Ann Liebert, Inc. Date: Sep 1, 2019.
Panoramica
È stato provato che PeriCam PSI è uno strumento utile in un’ampia gamma di campi nell’area della ricerca in ambito di neurovascolarizzazione e angiogenesi. Uno dei principali campi è la ricerca delle terapie proangiogeniche per arteriopatia periferica e guarigione delle ferite in modelli animali preclinici. Per la PAD, viene indotta chirurgicamente un’ischemia alle estremità inferiori, confermata utilizzando PeriCam PSI: in questo modo è possibile seguire il processo dinamico di recupero della perfusione nel tempo. Analogamente, si creano ferite cutanee e PeriCam PSI viene utilizzato per seguirne la normale guarigione. In entrambi i modelli, PeriCam PSI consente al ricercatore di seguire gli stessi soggetti, in maniera longitudinale, risparmiando tempo e denaro e riducendo il numero di animali necessari per uno studio.
Un altro campo è lo studio del cancro nel saggio CAM e nei modelli tumorali sottocutanei, nonché lo sviluppo di agenti antiangiogenici per il trattamento. PeriCam PSI può essere utilizzato per monitorare la perfusione nei tumori durante l’avanzamento di questi ultimi, oltre a valutare l’efficacia delle terapie mirate a indebolirli.
Ischemia degli arti inferiori (HLI)
La preparazione all’ischemia agli arti inferiori nei murini è comunemente utilizzata e rappresenta un modello importante per l’analisi dell’arteriopatia periferica. Coinvolge la legatura e l’escissione dell’arteria femorale unilaterale per indurre un’ischemia agli arti inferiori acuta, permettendo una valutazione della rigenerazione vascolare, dell’angiogenesi e dell’arteriogenesi grazie a diverse strategie, quali la presenza di un fattore di crescita e una terapia cellulare. Inoltre, può essere utilizzata per valutare gli effetti proangiogenici di agenti terapeutici 3-12 o un recupero naturale in animali sani 13 rispetto a quelli malati (diabetici) 14-16, quelli giovani rispetto a quelli adulti 17, nonché in animali di tipo selvatico rispetto a quelli geneticamente modificati 18-20.
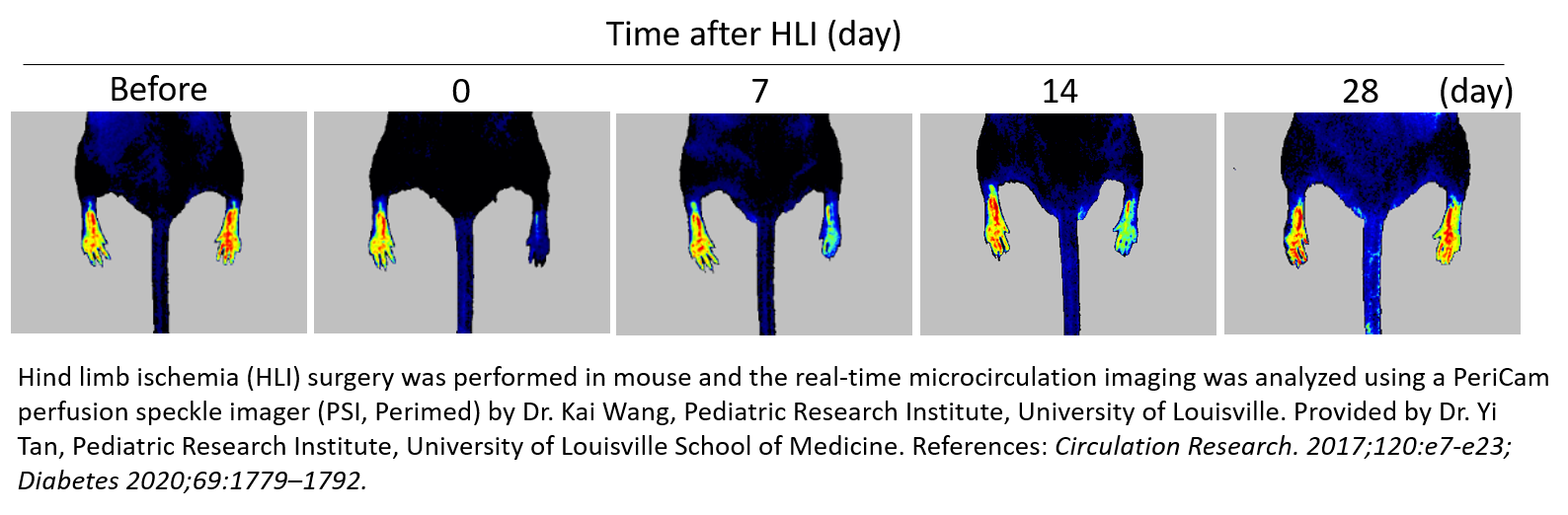
Il sistema PeriCam PSI con laser speckle contrast imaging è utilizzato per confermare un’ischemia post-chirurgica mediante misurazione di una riduzione della perfusione sanguigna nella microcircolazione (60-70%), nonché per monitorare in maniera longitudinale l’efficacia della strategia del trattamento. Generalmente, ogni animale viene seguito fino a un mese dopo il trattamento/il periodo post-intervento con il PSI, per documentare gli aumenti incrementali della perfusione sanguigna in seguito a rivascolarizzazione, consentendo di risparmiare tempo e denaro e riducendo il numero di animali necessari per lo studio.
Saggio membrana corio-allantoidea (CAM)
Durante lo sviluppo embrionale dei polli, la CAM si forma mediante fusione dello strato mesodermico dell’allantoide con lo strato mesodermico del corion. È una membrana altamente vascolarizzata, non innervata, extra embrionale: caratteristiche che la rendono un substrato ideale per l’analisi di angiogenesi e crescita dei tumori. Un uovo di pollo fertilizzato viene incubato dai quattro agli otto giorni, quando viene creata una finestra nel guscio per osservare la formazione dell’embrione e dei vasi sanguigni.
Per il saggio dell’angiogenesi, vari farmaci e biomolecole possono essere erogati a livello topico e analizzati per la loro potenza angiogenica. Inoltre, gli scaffold di biomateriali possono essere impiantati e monitorati per l’invasione vascolare nel tempo con lo scopo di valutare una strategia ingegneristica tissutale.
Per i modelli tumorali, diversi tipi di cellule tumorali possono essere trapiantati nel CAM per la crescita del tumore. Ciò fornisce un modello relativamente semplice per l’analisi delle formazioni di diversi tumori e consente di testare una nuova terapia farmacologica e strategie di trattamento personalizzate. Il modello CAM è altamente riproducibile, economico e non richiede approvazione dei comitati etici come tanti altri modelli animali in vivo. Inoltre, il modello CAM ha un’immunodeficienza naturale che lo rende ideale per il trasporto cellulare e il sistema chiuso prolunga l’emivita di varie molecole sperimentali, riducendo il numero di studi necessari.
Il sistema PeriCam PSI con laser speckle contrast imaging può essere utilizzato per misurare le variazioni nella perfusione sanguigna durante il saggio dell’angiogenesi e rilevare differenze nell’efficacia di vari composti proangiogenici. Può essere anche utilizzato per monitorare la formazione di vasi sanguigni intratumorali funzionali 25 e valutare l’efficacia di agenti antiangiogenici per il trattamento dei tumori.
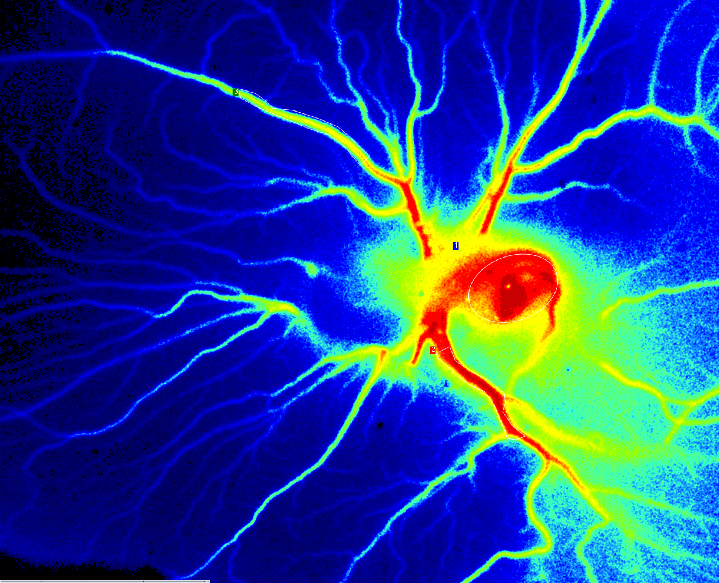
Perfusione PSI Z del giorno 6 del saggio CAM dopo la fecondazione.
Tumore sottocutaneo
La crescita e la metastasi di tumori dipendono dallo sviluppo dei vasi sanguigni e da una microcircolazione efficace. Senza angiogenesi, un piccolo gruppo di cellule tumorali non può crescere in un sito secondario. Poiché l’angiogenesi gioca un ruolo centrale nella crescita, nella progressione, nell’invasione e nella metastasi del tumore, inibendola fornisce una potenziale strategia per alcuni trattamenti tumorali.
Il modello di tumore sottocutaneo è il sistema di valutazione più comune per una valutazione in vivo di nuovi candidati farmaci anticancro. Generalmente, utilizzando specie animali con immunodeficienza, le cellule tumorali sottoposte a coltura vengono impiantate per via sottocutanea causando la formazione di tumori solidi in circa 2 settimane. Un’ampia varietà di linee cellulari cancerose umane e murine è stata adattata alla crescita in un ospite roditore e, pertanto, consente la valutazione di terapie nel modello tumorale pertinente. I ricercatori monitorano la crescita e la progressione tumorale e spesso eseguono un saggio della densità dei microvasi tumorali per valutare l’efficacia della strategia di trattamento. PeriCam PSI può essere utilizzato per monitorare nel tempo la perfusione sanguigna nei tumori sottocutanei e valutare l’efficacia delle terapie antiagiogeniche per il trattamento del cancro.
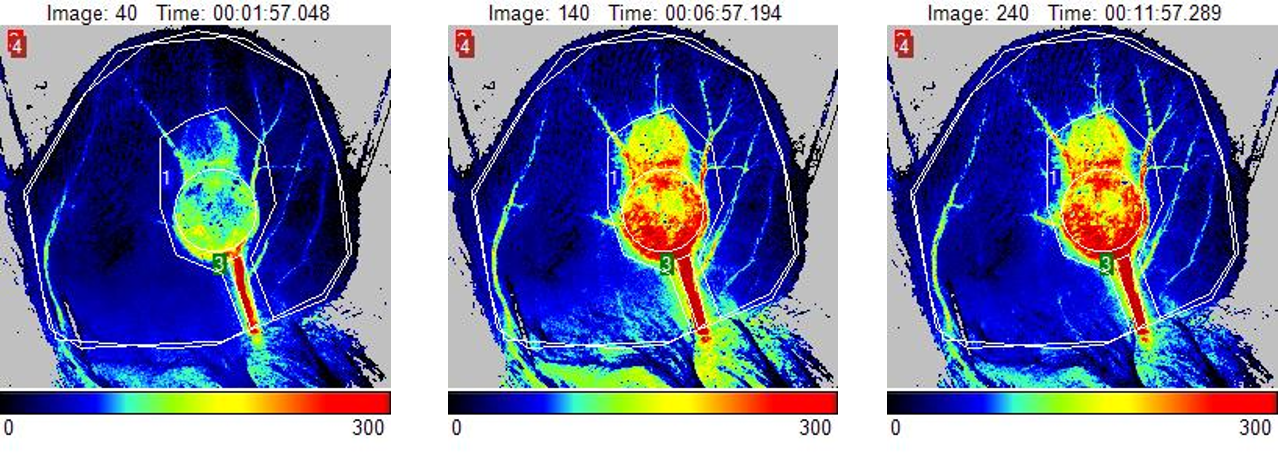
Immagini di perfusione dell’orecchio di un topo con tumore sottocutaneo al giorno 14. Le immagini riflettono un incremento della perfusione sanguigna del tumore in risposta a una stimolazione di calore.
References:
1. LED-Based Photoacoustic Imaging for Monitoring Angiogenesis in Fibrin Scaffolds. Yunhao Zhu, Xiaofang Lu, Xiaoxiao Dong, Jie Yuan, Mario L. Fabiilli, and Xueding Wang. 9, September 2019, Tissue Engineering Part C: Methods, Vol. 25, pp. 523-531.
2. Controlled release of basic fibroblast growth factor for angiogenesis using acoustically-responsive scaffolds. Alexander Moncion, Melissa Lin, Eric G. O’Neill, Renny T. Franceschi, Oliver D. Kripfgans, Andrew J. Putnam, Mario L. Fabiilli. 2017, Biomaterials, Vol. 140, pp. 26-36.
3. MiR-15b-5p Regulates Collateral Artery Formation by Targeting AKT3 (Protein Kinase B-3). Ling-Ping Zhu, Ji-Peng Zhou, Jia-Xiong Zhang, Jun-Yao Wang, Zhen-Yu Wang, Miao Pan, Ling-. May 2017, Arteriosclerosis, Thrombosis, and Vascular Biology, Vol. 37, pp. 957-968.
4. Precise and long-term tracking of adipose-derived stem cells and their regenerative capacity via superb bright and stable organic nanodots. Dan Ding, Duo Mao, Kai Li, Xiaomin Wang, Wei Qin, Rongrong Liu, David Shunzhong Chiam, Nikodem Tomczak, Zhimou Yang, Ben Zhong Tang, Deling Kong, Bin Liu. 12, 2014, ACS Nano, Vol. 8, pp. 12620-12631.
5. Extracellular Matrix Hydrogel Promotes Tissue Remodeling, Arteriogenesis, and Perfusion in a Rat Hindlimb Ischemia Model. Jessica L. Ungerleider, Todd D. Johnson, Melissa J. Hernandez, Dean I. Elhag, Rebecca L. Braden, Monika Dzieciatkowska, Kent G. Osborn, Kirk C. Hansen, Ehtisham Mahmud and Karen L. Christman. 1-2, 2016, JACC: Basic to Translational Science, Vol. 1, pp. 32-44.
6. Engineering an Injectable Muscle-Specific Microenvironment for Improved Cell Delivery Using a Nanofibrous Extracellular Matrix Hydrogel. Nikhil Rao, Gillie Agmon, Matthew T. Tierney, Jessica L. Ungerleider, Rebecca L. Braden, Alessandra Sacco, Karen L. Christman. 2017, ACS Nano, Vol. 11, pp. 3851-3859.
7. Marrow-isolated adult multilineage inducible cells embedded within a biologically-inspired construct promote recovery in a mouse model of peripheral vascular disease. Cristina Grau-Monge, Gaëtan J-R Delcroix, Andrea Bonnin-Marquez, Mike Valdes, Ead Lewis Mazen Awadallah, Daniel F Quevedo, Maxime R Armour, Ramon B Montero, Paul C Schiller, Fotios M Andreopoulos and Gianluca D’Ippolito. 1, 2017, Biomedical Materials, Vol. 12, p. 015024.
8. Natural compound bavachalcone promotes the differentiation of endothelial progenitor cells and neovascularization through the RORα-erythropoietin-AMPK axis. Shuang Ling, Rong-Zhen Ni, Yunyun Yuan, Yan-Qi Dang, Qian-Mei Zhou, Shuang Liang, Fujiang Guo, Wei Feng, Yuanyuan Chen, Katsumi Ikeda, Yukio Yamori, and Jin-Wen Xu. 49, 2017, Oncotarget, Vol. 8, pp. 86188-86205.
9. Topical tissue nano-transfection mediates non-viral stroma reprogramming and rescue. Daniel Gallego-Perez, Durba Pal, Subhadip Ghatak, VeysiMalkoc, Natalia Higuita-Castro, Surya Gnyawali, Lingqian Chang, Wei-Ching Liao, Junfeng Shi, Mithun Sinha, Kanhaiya Singh, Erin teen, Alec Sunyecz, Richard Stewart, JordanMoore, Thomas Ziebro, Robert. 2017, Nature Nanotechnology, Vol. 12, pp. 974-979.
10. In vivo efficacy of endothelial growth medium stimulated mesenchymal stem cells derived from patients with critical limb ischemia. Rida Al-Rifai, Philippe Nguyen, Nicole Bouland, Christine Terryn, Lukshe Kanagaratnam, Gaël Poitevin, Caroline François, Catherine Boisson-Vidal, Marie-Antoinette Sevestre & Claire Tournois. 17, 2019, Journal of Translational Medicine, Vol. 9, p. 261.
11. NFAT5 promotes arteriogenesis via MCP‐1‐dependent monocyte recruitment. Zhang, Xing‐Chi Lin Miao Pan Ling‐Ping Zhu Quan Sun Zheng‐Shi Zhou Chuan‐Chang Li Guo‐Gang. 2, 2020, Journal of Cellular and Molecular Medicine, Vol. 24.
12. MicroRNA-146a Regulates Perfusion Recovery in Response to Arterial Occlusion via Arteriogenesis. Heuslein Joshua L., McDonnell Stephanie P., Song Ji, Annex Brian H., Price Richard J. 2018, Frontiers in Bioengineering and Biotechnology, Vol. 6, p. 1.
13. Denervation in Femoral Artery-Ligated Hindlimbs Diminishes Ischemic Recovery Primarily via Impaired Arteriogenesis. Yinghuan Cen, Junfeng Liu, Yuansen Qin, Ruiming Liu, Huijin Wang, Yu Zhou, Shenming Wang, Zuojun Hu. 5, 2016, PLOS One, Vol. 11, p. e0154941.
14. Elevating CXCR7 Improves Angiogenic Function of EPCs via Akt/GSK-3β/Fyn-Mediated Nrf2 Activation in Diabetic Limb Ischemia. Xiaozhen Dai, Xiaoqing Yan, Jun Zeng, Jing Chen, Yuehui Wang, Jun Chen, Yan Li, Michelle T Barati, Kupper A Wintergerst, Kejian Pan, Matthew A Nystoriak, Daniel J Conklin, Gregg Rokosh, Paul N Epstein, Xiaokun Li, Yi Tan. 2017, Circulation Research, Vol. 120, pp. e7-e23.
15. Sitagliptin-mediated preservation of endothelial progenitor cell function via augmenting autophagy enhances ischaemic angiogenesis in diabetes. Dai, X., Zeng, J., Yan, X., Lin, Q., Wang, K., Chen, J., Shen, F., Gu, X., Wang, Y., Chen, J., Pan, K., Cai, L., Wintergerst, K. A. and Tan, Y. 1, 2018, Journal of Cellular and Molecular Medicine, Vol. 22, pp. 89-100.
16. Endothelial Overexpression of Metallothionein Prevents Diabetes-Induced Impairment in Ischemia Angiogenesis Through Preservation of HIF-1α/SDF-1/VEGF Signaling in Endothelial Progenitor Cells. Kai Wang, Xiaozhen Dai, Junhong He, Xiaoqing Yan, Chengkui Yang, Xia Fan, Shiyue Sun, Jing Chen, Jianxiang Xu, Zhongbin Deng, Jiawei Fan, Xiaohuan Yuan, Hairong Liu, Edward C. Carlson, Feixia Shen, Kupper A. Wintergerst, Daniel J. Conklin, Paul N. Epstein. 8, August 2020, Diabetes, Vol. 69, pp. 1779-1792.
17. DNA Methyltransferase 1–Dependent DNA Hypermethylation Constrains Arteriogenesis by Augmenting Shear Stress Set Point. Joshua L. Heuslein, Catherine M. Gorick, Ji Song, Richard J. Price. 12, 2017, Journal of the American Heart Association, Vol. 6.
18. Loss of Endothelial CXCR7 Impairs Vascular Homeostasis and Cardiac Remodeling After Myocardial Infarction. Huifeng Hao, PhD, et al. 2017, Circulation, Vol. 135, pp. 1253-1264.
19. Vascular growth responses to chronic arterial occlusion are unaffected by myeloid specific focal adhesion kinase (FAK) deletion. Joshua L. Heuslein, Kelsey P. Murrell, Ryan J. Leiphart, Ryan A. Llewellyn, Joshua K. Meisner & Richard J. Price. 2016, Scientific Reports, Vol. 6, p. 27029.
20. Despite Normal Arteriogenic and Angiogenic Responses, Hindlimb Perfusion Recovery and Necrotic and Fibro-Adipose Tissue Clearance Are Impaired in MMP9 Deficient Mice. Meisner JK, Annex BH, Price RJ. 6, 2015, Journal of Vascular Surgery, Vol. 61, pp. 1583–1594.
21. Cutaneous Epithelial to Mesenchymal Transition Activator ZEB1 Regulates Wound Angiogenesis and Closure in a Glycemic Status–Dependent Manner. Singh, Kanhaiya and Sinha, Mithun and Pal, Durba and Tabasum, Saba and Gnyawali, Surya C. and Khona, Dolly and Sarkar, Subendu and Mohanty, Sujit K. and Soto-Gonzalez, Fidel and Khanna, Savita and Roy, Sashwati and Sen, Chandan K. 11, 2019, Diabetes, Vol. 68, pp. 2175-2190.
22. Correction of MFG-E8 Resolves Inflammation and Promotes Cutaneous Wound Healing in Diabetes. A. Das, S. Ghatak, M. Sinha, S. Chaffee, Noha S. Ahmed, N. L. Parinandi, E. S. Wohleb, J. F. Sheridan, C. K. Sen, and S. Roy. 12, 2016, The Journal of Immunology, Vol. 196, pp. 5089-5100.
23. Circulating Exosomal miR-20b-5p Inhibition Restores Wnt9b Signaling and Reverses Diabetes-Associated Impaired Wound Healing. Yuan Xiong, Lang Chen, Chenchen Yan, Wu Zhou, Yori Endo, Jing Liu, Liangcong Hu,Yiqiang Hu, Bobin Mi and Guohui Liu. 3, 2020, Small, Vol. 16, p. 1904044.
24. Saliva Exosomes-Derived UBE2O Promotes Angiogenesis in Cutaneous Wounds by Targeting SMAD6. Bobin Mi, Lang Chen, Yuan Xiong, Chenchen Yan, Hang Xue, Adriana C. Panay, Jing Liu, Liangcong Hu, Yiqiang Hu, Yun Sun, Faqi Cao, Wu Zhou, Guohui Liu. 18, 2020, Journal of Nanobiotechnology, Vol. 6, p. 68.
25. Laser speckle contrast analysis (LASCA) technology for the semiquantitative measurement of angiogenesis in in-ovo-tumor-model. Eric Pion, Claudia Asam, Anna-Lena Feder, Oliver Felthaus, Paul I. Heidekrueger,Lukas Prantl, Silke Haerteis, Thiha Aung. 2020, Microvascular Research, Vol. 133, p. 104072.
Compilare il modulo per ottenere maggiori informazioni
Disclaimer: è possibile che non tutti i prodotti presenti sul sito Web di Perimed siano in vendita in tutti i mercati.



